イオン結晶

 NaCl型
NaCl型
Na+(黄色)とCl-(緑色)が単純立方格子の隅に交互に配列した結晶構造がNaCl型結晶構造(岩塩構造)である。NaCl型結晶構造では、1つのNa+に最近接するCl-は前後左右上下の6であり(これを配位数が6であるという)、当然ではあるが、1つのCl-に最近接するNa+も6である。NaCl型結晶構造の単位格子の構造の表し方は2つ可能である。それは下に示したように単位格子の立方体面の中心(面心)と各頂点にCl-を置く構造のものと、逆に面心と頂点にNa+(黄色)を置く構造のものであるが、当然ながらこの2つは等価である。
 |  |
| NaCl型結晶構造 | 単位格子の構造 |
 CsCl型
CsCl型
CsCl型結晶は、一方のイオン(下の図では紫色のCs+)が立方格子の中心(体心)に配置し、もう一方のイオン(緑色はCl-)が8つの頂点に配置するような形で次々に繋がった構造をとっている。Cs+とCl-が等価の位置関係にあることは、下の左の図(結晶構造を部分的に眺めたもの)を見ると、Cl-(緑玉)を体心の位置として捉えると、その立方体の8つの頂点にCs+(紫玉)が配置されることになることで理解できると思う。因みに、CsCl型結晶の配位数は8である。
 |  |
| 単位格子の構造 | Cl-を体心にすると・・・ |
 閃亜鉛鉱型
閃亜鉛鉱型
閃亜鉛鉱(ZnS)型結晶は、ダイヤモンド型結晶構造(右端)で最近接原子(イオン)を別種の原子(イオン)で置換したものであり、配位数は4。単位格子に含まれる陽イオンと陰イオンはそれぞれ4である。
 蛍石(フッ化カルシウム)型
蛍石(フッ化カルシウム)型
蛍石(フッ化カルシウム、CaF2)型結晶は、下の写真で青色のStrutで示された立方体(立方体を丁度形成できるStrutが今のところZomeには用意されていないので、途中切れた2本の青色Strut 2本で立方体の1辺となる)を8等分した小立方体の中心にカルシウムイオン(青緑色の玉が Ca2+)が配置され、大立方体には合計4つ含まれており、大立方体の各面心と各頂点にフッ化物イオン(黄色の玉が F-)が配置される結晶構造をとっている。
単位格子には、Ca2+が8個、 F-(フッ化物イオンだけを考えると面心立方格子が形成される)が4個含まれている。Ca2+に配位する F- は4個で、F-に配位するCa2+は8個ある。
 ルチル型
ルチル型
二酸化チタン(TiO2)の結晶の1つに金紅石(ルチル)がある。写真でチタンイオン(Ti4+)は青、酸化物イオン(O2-)は赤である。単位格子の中心にある青色のTi4+に6個の赤色のO2-が配位している。本来、この6つの赤玉は中心の青玉と等距離にあるが、Zomeではそれが構築できなかったので、青色と緑色の違った長さのStrutで繋げてある。
 ペロフスカイト構造(理想型)
ペロフスカイト構造(理想型)
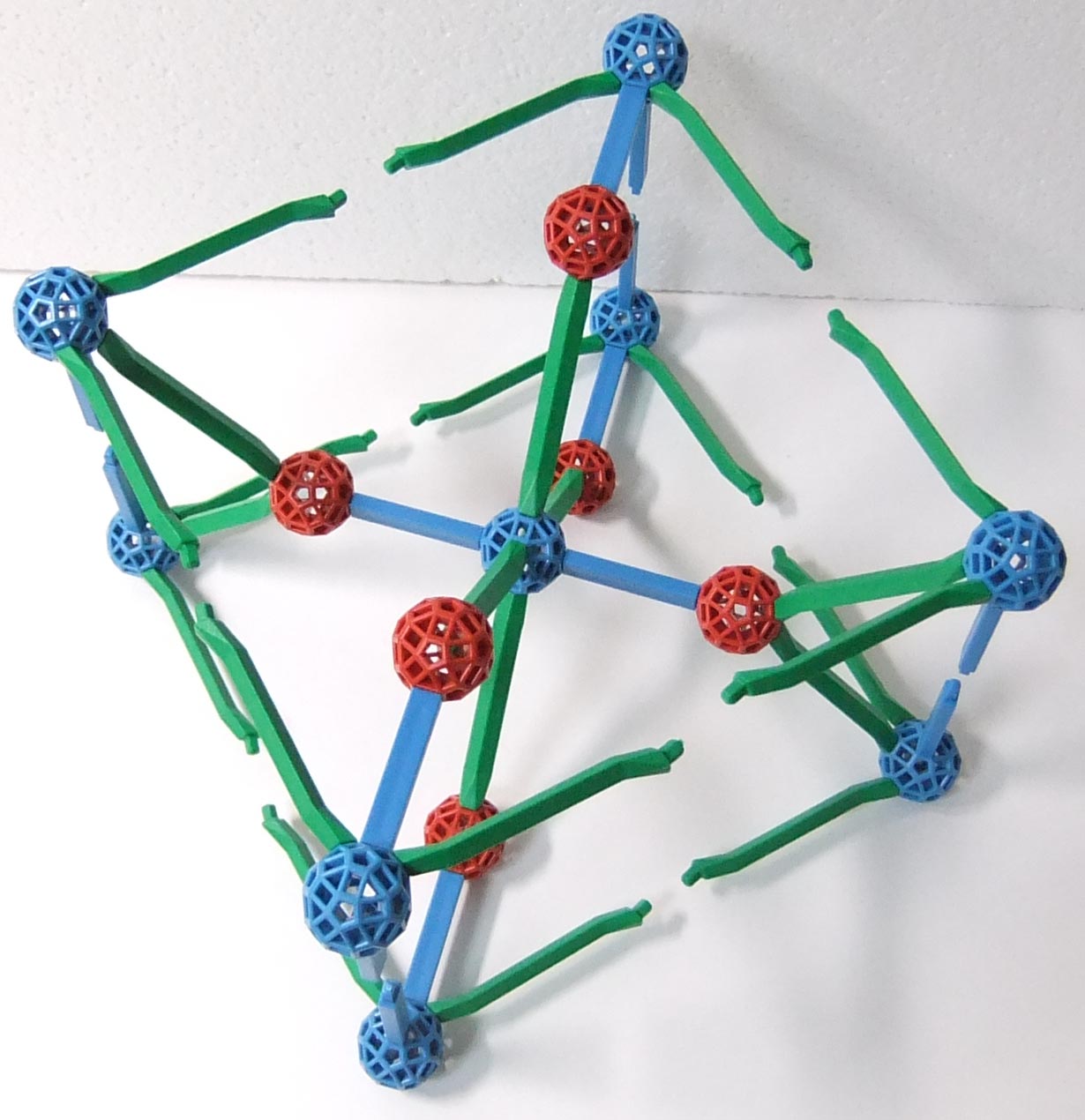
ペロフスカイト(perovskite)は、灰チタン石と呼ばれ、理想化学組成は CaTiO3 である。その結晶構造はペロフスカイト構と呼ばれ、高温では立方晶系の理想型構造であるが、室温では歪んだペロフスカイト構造を取り、斜方晶系となる。次の写真は理想型のペロフスカイト構造をZomeで組み立てたものである。立方体の中心にあるオレンジ色の玉がCa2+で、各辺の中心にある赤色の玉がO2-、各頂点に位置する青色の玉がTi4+である。写真を見て分かるように、この構造では、Ca2+に12個のO2-が配位し、Ti4+には6個のO2-が配位している。



 NaCl型
NaCl型

 CsCl型
CsCl型

 閃亜鉛鉱型
閃亜鉛鉱型


 蛍石(フッ化カルシウム)型
蛍石(フッ化カルシウム)型

 ルチル型
ルチル型

 ペロフスカイト構造(理想型)
ペロフスカイト構造(理想型)

